 接受細胞移植者之所以產生免疫排斥反應,係因被移植的細胞表面抗原會遭受接受者免疫系統辨識,被視為入侵者而誘發免疫排斥反應。此現象無論在同種移植(allograft)或是異種移植(xenograft)均存在。細胞表面有三種免疫抗原分子在細胞移植時扮演重要角色,例如主要組織相容性複合抗原(major histocompatibility complex antigens,MHC)、次要組織相容性複合抗原(minor histocompatibility antigens,mHAgs)以及ABO血型抗原(Watkins, 2001;Roopenian et al., 2002)。胚幹細胞及其分化後的衍生細胞亦具有細胞表面抗原,因此胚幹細胞移植時的免疫排斥問題是臨床應用的重要課題。Drukker等人(2002)指出,人類胚幹細胞在未分化階段的MHC-I表現量很低,然而當胚幹細胞分化形成胚體(embryoid body,EB)後,其MHC-I表現量增加2~4倍,並且在誘導形成畸胎瘤(teratoma)後,MHC-I表現量更是增加了8~10倍;雖然胚幹細胞從未分化階段進行到分化階段的MHC-I表現量有增加趨勢,然而表現量之絕對值仍低於體細胞(如HeLa細胞)的表現量。
接受細胞移植者之所以產生免疫排斥反應,係因被移植的細胞表面抗原會遭受接受者免疫系統辨識,被視為入侵者而誘發免疫排斥反應。此現象無論在同種移植(allograft)或是異種移植(xenograft)均存在。細胞表面有三種免疫抗原分子在細胞移植時扮演重要角色,例如主要組織相容性複合抗原(major histocompatibility complex antigens,MHC)、次要組織相容性複合抗原(minor histocompatibility antigens,mHAgs)以及ABO血型抗原(Watkins, 2001;Roopenian et al., 2002)。胚幹細胞及其分化後的衍生細胞亦具有細胞表面抗原,因此胚幹細胞移植時的免疫排斥問題是臨床應用的重要課題。Drukker等人(2002)指出,人類胚幹細胞在未分化階段的MHC-I表現量很低,然而當胚幹細胞分化形成胚體(embryoid body,EB)後,其MHC-I表現量增加2~4倍,並且在誘導形成畸胎瘤(teratoma)後,MHC-I表現量更是增加了8~10倍;雖然胚幹細胞從未分化階段進行到分化階段的MHC-I表現量有增加趨勢,然而表現量之絕對值仍低於體細胞(如HeLa細胞)的表現量。目前,一般認為避開免疫排斥問題最有效的辦法是以患者本身的細胞,利用體細胞核轉置技術平台,建立同源性胚幹細胞株後再進行自體移植(autograft)。雖然體細胞核轉置技術提供建構醫療性複殖的遠景,並可建立專屬於個人免疫完全相容性之胚幹細胞株,然而仍存在著技術、倫理與道德等問題猶待克服。目前以人類胚幹細胞做為臨床醫療應用仍有三項技術有待挑戰:(1)幹細胞移植需克服免疫排斥問題;(2)人類胚幹細胞的繼代與培養須於無非人類之動物性污染源的環境中;(3)利用特定誘導技術將胚幹細胞分化成為特定的細胞型態,且不帶有致癌性的細胞。為了克服免疫排斥的問題,有學者相繼提出五個主要降低或免除免疫作用的策略,包括有:(1)將胚幹細胞移植於免疫特許區,例如大腦或是睪丸等部位;(2)建立人類胚幹細胞之免疫表現型(immunophenotype)資料庫,以及與病人MHC完全相容之胚幹細胞株;(3)藉由遺傳學技術操控胚幹細胞MHC與免疫調節因子之表現;(4)藉由同種提供者進行同種移植技術;(5)產製醫療性複殖相容性之細胞株(Drukker, 2008)。
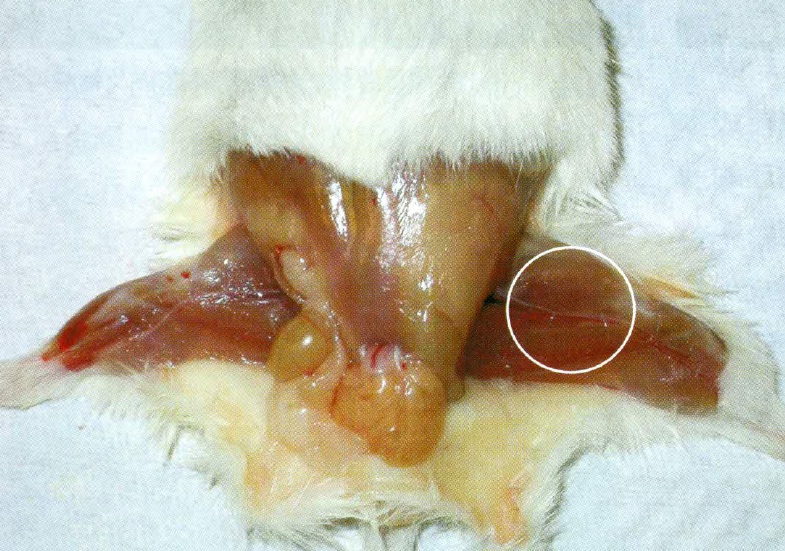
另一方面,胚幹細胞之腫瘤生成性一直以來是胚幹細胞移植試驗的隱憂。幹細胞移植後所產生的畸胎瘤,在人類胚幹細胞與小鼠胚幹細胞移植試驗中均已被發現(Amit et al., 2004;Bulić-Jakus et al., 2006;Blum et al., 2008)。然而,在猪胚幹細胞移植試驗中,僅有一篇研究報告指出有畸胎瘤之形成(Hochereau-de Reviers and Perreau, 1993),該報告中指出當猪胚幹細胞若源自於較晚期的囊胚(第10~11天),則進行移植時會產生畸胎瘤;但若衍生自早期囊胚(第5~6天)所建立的猪胚幹細胞,則不容易形成畸胎瘤。此結論在Anderson等人(1994)的報告中獲得驗證,且在吾等研究中,以豬胚幹細胞進行嚴重免疫不全小鼠(severe combined immunodeficiency,SCID)後腿肌肉(圖1),以及SD大鼠(Sprague-Dawley)腦部(圖2)移植時,均未見畸胎瘤之研究結果相同(Yang et al., 2009; 2010)。因此,以猪胚幹細胞移植的試驗模式,探討細胞分化程度對接受者免疫耐受性與免疫排斥反應之關係,並克服或減低接受者免疫反應,將有助於胚幹細胞移植治療之發展與應用。
相關照片
大家覺得這篇文章
一級棒:65%
我喜歡:11%
很實用:19%
夠新奇:2%
普普啦:4%
看過這篇文章的人說
登入會員即可參加留言
婧(達人級會員)發表於 114/12/23
讚
Malain(達人級會員)發表於 114/09/09
讚
Augustine Chao(進階級會員)發表於 114/08/23
Good
帥帥平(進階級會員)發表於 114/08/21
讚
陸志平(高手級會員)發表於 114/08/21
感謝分享
Mika Mike(高手級會員)發表於 114/08/04
謝謝分享

早晨微風(達人級會員)發表於 110/04/27
謝謝
洛奇亞(達人級會員)發表於 110/01/26
棒
buzz(入門級會員)發表於 109/10/19
專業
陳*杰(達人級會員)發表於 105/05/24
很好